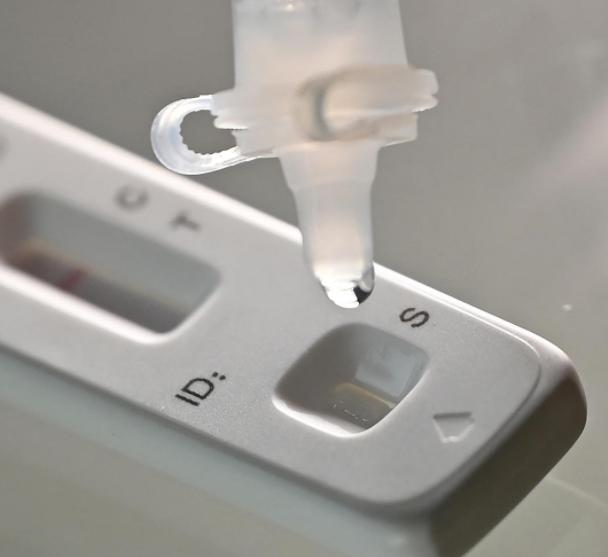
12. märtsilth 2022, aNMPA (SFDA) väljastas teatise, millega kiideti heaks Nanjing Vazyme Biotechi COVID-19 antigeenitoodete enesetestimise taotluse muudatusCo., Ltd, Pekingi Jinwofu biotehnoloogia tehnoloogiaCo., Ltd, Shenzhen Huada Yinyuan Pharmaceutical Technology Co., Ltd, Guangzhou Wondfo Biotech Co., Ltd jaBeijing Savant Biotechnology Co., Ltd(Huaketai).Müügile on toodud viis COVID-19 antigeeni enesetestimise toodet.
11. märtsil 2022 teatas NHC, et uudse koroonaviiruse testimisstrateegia edasiseks optimeerimiseks ning COVID-19 ennetamise ja tõrje vajaduste rahuldamiseks otsustas Riigivolikogu ühise ennetus- ja kontrollimehhanismi terviklik meeskond lisada antigeeni testimine nukleiinhapete testimiseks ja „uudse koroonaviiruse antigeeni tuvastamise rakendusprotokoll (katseversioon)”
Protokoll määrab antigeeni testimiseks kohaldatava populatsiooni:
Esiteks need, kes külastavad esmaseid meditsiiniasutusi ja kellel on sümptomid nagu hingamisteed ja palavik 5 päeva jooksul alates sümptomite ilmnemisest;
Teiseks karantiinivaatluspersonal, sealhulgas kodukarantiini vaatlus, lähikontakt ja lähikontakt, sisenemise karantiinivaatlus, isoleeritud ala ja kontrollpiirkonna töötajad;
Kolmas on kogukonna elanikud, kellel on vajadus antigeeni enesetuvastuse järele.
Nõuanded: Antigeeni tuvastamine on nukleiinhapete tuvastamise oluline täiendus, kuid antigeeni enesetuvastuse tulemusi ei saa kasutada infektsiooni diagnoosimise aluseks.
Postitusaeg: 22. märts 2022